圖像來源/iStock.com/libre de droit
近年來,乳癌一直是國內婦女癌症的頭號威脅,且好發年齡更有年輕化的趨勢。乳癌主要有4種不同的分類亞型,所使用的治療方式也不盡相同。除了15-20%為第二型人類上皮生長受體(HER2)過度表現型(HER2+)外,另約有10-20%的乳癌是二種荷爾蒙受體—雌激素(ER)/黃體素(PR)和HER2都是陰性,稱為三陰性乳癌(triple-negative breast cancer, TNBC),這類病人對荷爾蒙治療的效果最不好,在治療上特別棘手。
為何特別棘手?由於三陰性乳癌缺乏明確受體,無法有一個「目標對象」使荷爾蒙療法或標靶藥物治療來抑制癌細胞,所以導致治療方式相當有限,目前病人只有使用化學治療的選擇。然而,在三陰性乳癌的病人常發現BRCA基因的突變,尤其是BRCA1更為常見,使得病人在化療後常面臨預後不佳、復發率高、腫瘤容易轉移到腦部、死亡率偏高,治療效果不如預期。因此亟需發展「新穎療法」,以得知三陰性乳癌真正發生的成因,期待能有較佳的療效和改善病人的預後結果。
國衛院分子基因所徐欣伶博士研究團隊,長期致力於研究三陰性乳癌。她們發現了一個稱為MCT-1的致癌基因,能調控細胞生長週期。MCT-1來自人類淋巴瘤T細胞株,經許多臨床病理數據證實,MCT-1基因高度表達於人類乳腺癌、侵略性瀰漫淋巴瘤與各種肺腺癌。因此,研究團隊進一步研究MCT-1致癌基因在乳癌的致病機轉,結果發現:
- 高表達的MCT-1蛋白會促使乳腺細胞有絲分裂異常,造成乳腺細胞癌化、乳腺小管分化異常而無法形成乳腺管,細胞異常增殖,走向癌組織。
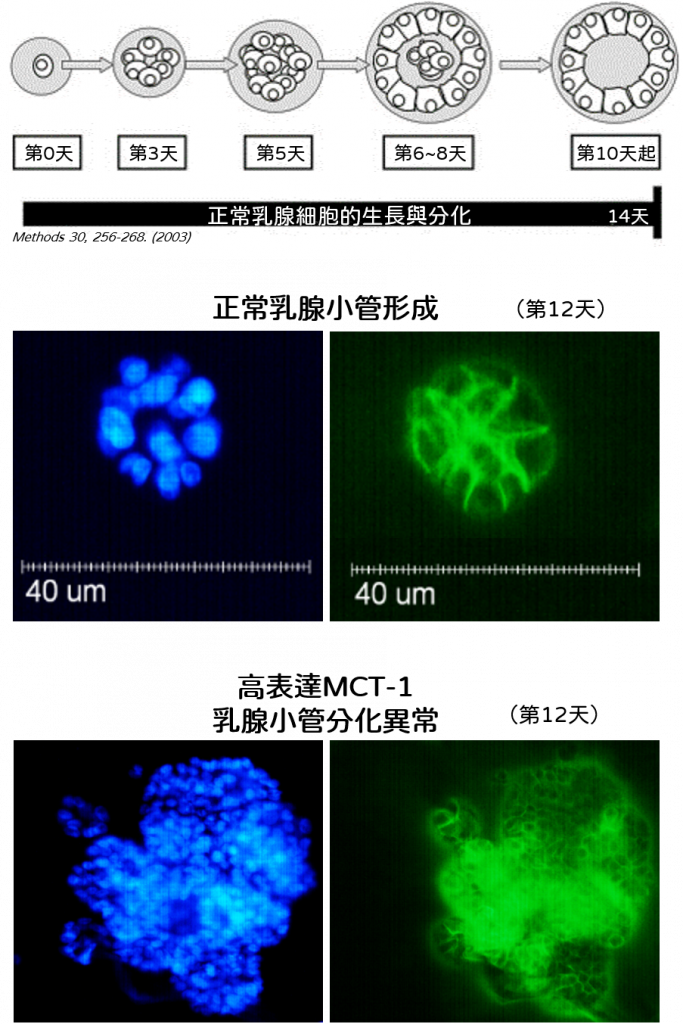
- 如果有一顆正常乳腺細胞變成高表達MCT-1時,它的移動與穿透能力會增加,並且進一步增強乳癌細胞的侵襲能力。
- 在臨床乳癌病人發現,高表達MCT-1的乳癌病人存活率較低,並有較高的乳癌復發率和死亡率。推斷乳癌病人存活率與MCT-1致癌基因的表達程度有關係。
- 高表達MCT-1致癌基因會促使三陰性乳癌細胞分泌發炎因子IL-6,IL-6與IL-6R結合後會引發一系列的發炎反應,不僅造成癌細胞增生並破壞細胞周邊組織微環境,同時將免疫系統中的巨噬細胞變壞,從M1型轉變成抑制免疫反應的M2型,幫助癌細胞的發展。此外,MCT-1與IL-6也會增加乳癌幹細胞數目和活性,導致三陰性乳癌的病程持續惡化。
- 在細胞與實驗動物模式結果發現,高表達MCT-1的乳癌組織明顯比對照組長得大、移動得快,表示高表達MCT-1會促使三陰性乳癌生長及轉移;反之,當抑制MCT-1,即乳癌細胞缺乏MCT-1時,三陰性乳癌的移動及侵襲能力均明顯降低。
因此,研究團隊發現,透過抑制三陰性乳癌細胞的MCT-1表現量,能夠降低巨噬細胞M1型轉M2型的機率,並且削弱癌細胞轉移與侵襲的能力。同時,也能減少乳癌幹細胞的自我更新能力,降低發生腫瘤細胞在複製與分裂時所產生的基因變異、抗藥性和癌症復發的機率。
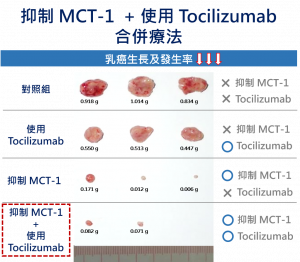
另一方面,她們也從抑制IL-6結合IL-6R著手,以阻斷後續的一系列發炎反應和訊息傳遞的發生。研究團隊利用一個用於治療原發性或類風濕性關節炎的IL-6R抗體藥「tocilizumab」來做合併治療,它可以和IL-6競爭,減少IL-6與IL-6R的結合機會。當在她們合併使用「抑制MCT-1活性」和「tocilizumab」的免疫療法後發現:
- 能有效阻止乳癌細胞生長;
- 顯著減少乳癌幹細胞族群;
- 高效率抑制三陰性乳癌發展;
- 增加M1型巨噬細胞以及改善腫瘤組織微環境。
徐博士研究團隊除了發現MCT-1致癌基因可作為三陰性乳癌臨床診斷與治療的生物標記,更找到tocilizumab藥物的新用途,建立了侵襲性乳癌新穎合併免疫療法。期盼這項三陰性乳癌治療的新策略,不僅能提供病人更多臨床治療的選擇,也能發揮更好的治療效果。
參考資料:
撰文者/劉盈秀、李岳倫 |圖片後製/劉盈秀
資料及圖片來源/徐欣伶
